Objetivo: A insuficiência renal aguda (IRA) no pós-operatório (PO) de cirurgia cardíaca é complicação grave. O objetivo deste trabalho é avaliar o tempo de circulação extracorpórea (CEC) como fator de risco para IRA.
Método: Foram avaliados 116 pacientes de um único centro, submetidos a cirurgia cardíaca com CEC. Foram avaliados os dados demográficos, características clínicas, variáveis intra e pós-operatórias. A creatinina sérica e o clearance de creatinina foram avaliados até o 5ºPO. IRA foi definida como necessidade de diálise. Os pacientes foram estratificados em dois grupos: grupo CEC£ 70 min e grupo CEC³90min.
Resultados: O aumento médio da creatinina sérica no PO foi 0,18+0,41 no grupo CEC£70min e 0,42+0,44 no grupo CEC³90min (p=0,005). Diálise foi necessária em 1,3% dos pacientes do grupo CEC£70min, e em 12,5% do grupo CEC³90min (p=0,018). O risco relativo para diálise foi 1,12 (IC 95%, 1,00-1,20) para CEC³90min. Não houve diferença para mortalidade (5,2 versus 7,5%, p=0,631).
Conclusão: O desenvolvimento de IRA no pós-operatório de cirurgia cardíaca foi observado em pacientes com tempo de CEC superior a 90 minutos, embora o clearance de creatinina não tenha demonstrado alteração entre os grupos.
Objective: Acute renal failure following heart surgery is a major complication. The aim of this study was to evaluate if duration of cardiopulmonary bypass (CPB) is an important factor that influences kidney dysfunction.
Methods: One hundred and sixteen patients from a single center referred for heart surgery were evaluated. Demographic factors, clinical data, operative and postoperative variables were evaluated. Serum creatinine and creatinine clearance were calculated until the fifth postoperative day. Acute renal failure was defined as the requirement of dialysis therapy. Patients were divided into two groups, the CPB £70min Group, patients with CPB duration equal to or less than 70 minutes and the CPB³ 90min Group, patients with CPB duration equal to or more than 90 minutes.
Results: The median increases in serum creatinine were 0.18 + 0.41(CPB£70min) and 0.42 + 0.44 (CPB³ 90min - p=0.005). Dialysis was indicated in 1.3% (CPB£70min) and 12.5% (CPB³ 90min - p = 0.018). The odds ratio for dialysis was 1.12 (95% CI; 1.00-1.20) for CPB³ 90min. There was no significant difference in mortality (5.2 versus 7.5%, p = 0.631).
Conclusion: The greatest likelihood of developing kidney failure after heart surgery is observed when CPB is at least 90 minutes, although creatinine clearance was not significantly altered between the groups studied.
INTRODUÇÃO
A disfunção renal no pós-operatório de cirurgia cardíaca é fator de risco para mortalidade hospitalar e menor sobrevivência [1,2]. É complicação freqüente no pós-operatório de cirurgia cardíaca, com incidência relatada entre 1% e 31% [3-7]. As causas para disfunção renal são multifatoriais, sendo que a circulação extracorpórea (CEC)[8] apresenta efeitos deletérios na função renal [9]. O estado não fisiológico da CEC ativa as cascatas inflamatórias e anormalidades da coagulação que alteram a função renal. Pacientes com disfunção renal prévia quando submetidos a cirurgia cardíaca apresentam progressão da lesão renal com influência na sobrevida tardia [10,11].
O objetivo deste estudo é avaliar a influência do tempo de circulação extracorpórea como fator de risco para alteração da função renal.
MÉTODO
Foram avaliados, de forma prospectiva e consecutiva, os pacientes submetidos a cirurgia cardíaca no Hospital de Base da 7° Região, em Bauru, São Paulo, no período de janeiro a agosto de 2003. O Comitê de Ética local aprovou a realização do estudo. Os critérios de exclusão foram idade menor que 18 anos e insuficiência renal pré-operatória com necessidade de diálise.
Anestesia
Indução e manutenção da anestesia foram realizadas com sulfentanila (0,5 a 0,9 µg/kg seguidos de 0,4 a 0,8µg/kg/h) e midazolam (0,05 a 0,1 mg/kg seguidos de 0,1mg/kg/h). Isoflurano suplementar (0,5 a 1,0%) foi administrado por via inalatória. Brometo de pancurônio (0,1 mg/kg) foi utilizado como relaxante muscular.
Na sala de operações, foi realizada monitorização com eletrocardiograma contínuo pelas derivações DII e V5 (MPC-10, TEB, São Paulo, Brasil), com oximetria e com capnografia (DX-7100, Dixtal, São Paulo, Brasil). A pressão arterial média (PAM), obtida por dissecção da artéria radial, também foi monitorada (UM62009, Braile Biomédica, São José do Rio Preto, Brasil). Acesso venoso central foi providenciado por dissecção venosa da veia cubital ou punção da veia subclávia direita. Foi utilizado termômetro digital (UM62009, Braile Biomédica, São José do Rio Preto, Brasil) na avaliação da temperatura nasofaríngea.
Circulação extracorpórea
Anticoagulação foi realizada com heparina sódica para manutenção do tempo de coagulação ativado superior a 480s. O circuito de CEC foi preenchido com 1,8L de solução de Ringer lactato, 50 ml de manitol a 20%, 10 ml de gluconato de cálcio a 10%, 10 ml de sulfato de magnésio a 10%, 500mg de hidrocortisona, 750mg de cefuroxima e 5000UI de heparina.
Durante a CEC, foi realizada hipotermia a 32ºC, com fluxo arterial não pulsátil de 2,4L/min/m2 e pressão de perfusão entre 60 e 80 mmHg. Proteção miocárdica foi realizada com cardioplegia sangüínea hipercalêmica anterógrada intermitente. Foi realizada transfusão sanguínea, durante a CEC, para manutenção de hematócrito acima de 17%. No processo de interrupção da CEC, manteve-se a PAM acima de 65mmHg. O coração foi assistido por marca-passo externo quando a freqüência cardíaca foi menor que 70bpm. Foi administrada dobutamina rotineiramente, com dose inicial de 3µg/kg/min. Noradrenalina foi utilizada se a PAM fosse menor que 65mmHg. Foi administrada protamina (1mg para cada 100 UI de heparina). Foi realizada antibioticoterapia profilática com cefuroxima por 48 horas no PO.
Variáveis analisadas e definições
As variáveis avaliadas foram idade, peso, altura, superfície corpórea, sexo, tempo de perfusão, tempo de anóxia, tipo de cirurgia, menor hematócrito durante a CEC, presença de hipertensão arterial sistêmica, diabetes mellitus, doença vascular periférica e infarto do miocárdio prévio.
A creatinina sérica pré-operatória (CrPré) foi determinada antes da cirurgia. A creatinina sérica pós-operatória foi avaliada no 1º, 2º e 5º dias de pós-operatório. A creatinina pico pós-operatória (CrPós) foi definida como o maior valor de creatinina sérica determinada no pós-operatório. A diferença em percentual da creatinina (%DCr) é definida como a diferença da CrPré e CrPós representada em porcentagem da CrPré.
O clerance de creatinina estimado foi calculado pela fórmula de Cockroft-Gault: clearance de creatinina=(140-idade) x peso (kg)/(creatinina sérica x 72 [x0,85 para mulheres]).
O clerance de creatinina foi calculado no pré-operatório, 1º, 2º e 5º pós-operatórios.
Quando necessário, foi realizada hemodiálise para o tratamento da hiperpotassemia, da hipervolemia, da uremia ou acidose metabólica por insuficiência renal aguda (IRA)
Estratificação dos grupos
Os pacientes foram estratificados pelos critérios de Boldt et al. [12], em dois grupos, grupo CEC£70 minutos, composto por pacientes cujo tempo de CEC foi menor ou igual a 70 minutos, e , grupo CEC³90 minutos, composto por pacientes com tempo de CEC maior ou igual a 90 minutos.
Análise estatística
Os dados das variáveis contínuas são apresentados na forma de média+desvio padrão. Variáveis ordinais são apresentadas na forma de freqüência (%). O teste de qui-quadrado ou teste exato de Fischer foi utilizado para a análise das variáveis ordinais. Os grupos foram comparados pelo teste T Student para amostras não pareadas. A análise de variância de duplo fator para medidas repetitivas com análise post-hoc de Bonferroni foi utilizada na análise do clearance de creatinina dentro de cada grupo. O nível de significância estabelecido foi de 5%. Foi utilizado o programa de análise estatística SPSS® versão 11.0 (SPSS, Chicago, IL, EUA).
RESULTADOS
Foram avaliados 116 pacientes submetidos a cirurgia cardíaca com CEC no período e excluídos 28 pacientes que apresentaram tempo de CEC entre 70 e 90 minutos.
Para todos os pacientes, a idade média foi de 56,74+15,37 anos, sendo 56 mulheres, com tempo médio de CEC de 74,70+29,44 minutos. Foram realizadas 91 revascularizações do miocárdio e 25 cirurgias valvares.
As características demográficas e variáveis intra-operatórias para os grupos são demonstradas na Tabela 1. Os dados pós-operatórios estão na Tabela 2, na qual é observado aumento da creatinina sérica em 0,18+0,41 para grupo CEC£70min e 0,42+0,44 para o grupo CEC³90min (p=0,005). Também observa-se que a Dcreat% foi de 117,90+32,39% e 138,46+42,21% para os grupos (p=0,004).
A Figura 1 demonstra o clearance de creatinina de acordo com o dia da cirurgia para os grupos. Não houve diferença estatística entre o ClCreatbasal e o ClCreat5PO (p>0,05) para os dois grupos.
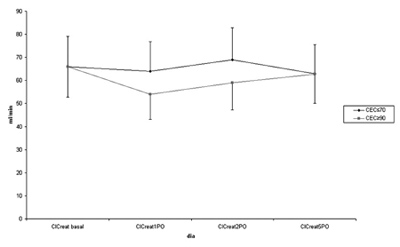
Fig. 1 - Alteração do clearance de creatinina
ClCreatbasal=clearance de creatinina pré-operatório, ClCreat1PO=clearance de creatinina no primeiro pós-operatório, ClCreat2PO=clearance de creatinina no segundo pós-operatório, ClCreat5PO=clearance de creatinina no quinto pós-operatório
Houve diferença estatística (p=0,018) para IRA entre os grupos. O grupo CEC³90min apresentou 12,5% de incidência versus 1,3% do grupo CEC=70min. O odds ratio para diálise foi 10,71(95% IC, 1,20-95,18).
DISCUSSÃO
Este estudo observacional avaliou a influência do tempo de CEC na função renal pós-operatória e no desenvolvimento de IRA. Foi observado que o tempo de CEC correlacionou-se com disfunção renal no pós-operatório e com incremento na necessidade de diálise.
Idade avançada, diabetes mellitus, disfunção renal pré-operatória, doença vascular periférica e peso corpóreo são conhecidos fatores de risco pré-operatório no desenvolvimento de IRA [6,13-15]. Apesar da ampla utilização da cirurgia cardíaca sem CEC e do emprego de novos equipamentos e fármacos na prevenção da disfunção renal pós-operatória, a incidência de insuficiência renal permanece elevada, sendo a IRA um problema desafiador em cirurgia cardíaca [16,17].
A CEC desencadeia importante resposta inflamatória em cirurgia cardíaca [18,19], sendo observado que é significativamente menor quando o tempo de CEC é inferior a 70 minutos [20]. A disfunção renal em cirurgia cardíaca avaliada pelo tempo de CEC em até 70 minutos ou superior a 90 minutos foi analisada em pacientes com creatinina sérica em até 200mmoL/dL (1,7mg/dl) no pré-operatório. Neste estudo, foram avaliados 100 pacientes até o 2ºPO, tendo sido relatadas alterações de enzimas tubulares renais, como a N-aceti-ß-galactosaminidase e gluationa transferase [12]. A evolução da creatinina sérica e clearance, em nosso estudo, foi realizada até o 5ºPO e foi utilizada diálise como critério para IRA. Ainda, deve ser considerado que 12,9% de nossos pacientes apresentam creatinina sérica maior que 1,7mg/dL.
Também foi observada a influência negativa do tempo de CEC na função renal pelo aumento da creatinina sérica, da variação da creatinina sérica e maior incidência de diálise em pacientes com tempo de CEC maior que 90 minutos. O odds ratio foi superior a 10 vezes para diálise entre os grupos, sendo consoante com um estudo multicêntrico, com mais de 2400 pacientes, que excluiu pacientes com creatinina sérica pré-operatória superior a 2,0mg/dl, e relatou que, quando o tempo de CEC é superior a 3 horas, o risco de IRA é 4 vezes superior ao limite de 2 horas [3].
O maior tempo de CEC possibilita o aumento no risco de hipotensão arterial com hipoxemia renal local pela maior exposição à CEC [3,13-14]. Ainda, o maior tempo de CEC está associado ao aumento de citocinas pró-inflamatórias como o TNF-a, IL-1, IL-6 e endotoxinas, que podem explicar a lesão tubular e deterioração da função renal [12,20].
Durante a CEC, episódios de embolia devem ser considerados como fator de risco potencial para infartos renais e conseqüente diminuição da função renal [21,22]. Recentemente, tem sido discutido se a não utilização da CEC preserva a função renal na revascularização do miocárdio [23]. Marcadores sensíveis de lesão tubular renal, como o N-acetil-ß-D-glucosaminidase, estão aumentados em pacientes com CEC [24]. Uma recente metanálise demonstrou que diálise é menos freqüente em pacientes submetidos a revascularização do miocárdio sem CEC [16].
São várias as limitações deste estudo. Primeiro, trata-se de estudo observacional em um único centro. Segundo, a amplitude de variação dos resultados das variáveis pode conduzir a erros que não demonstraram correlação, apesar de significativas. Terceiro, os dados apresentados não permitem avaliar a duração da CEC, do fluxo e da pressão de perfusão independentemente. Finalmente, o tratamento dialítico pode ter sido iniciado após o 5º dia de pós-operatório.
CONCLUSÃO
O desenvolvimento de IRA no pós-operatório de cirurgia cardíaca foi mais freqüente em pacientes com tempo de CEC superior a 90 minutos, quando comparado ao grupo menor que 70 minutos.
REFERÊNCIAS
1. Hirose H, Amano A, Yoshida S, Takahashi A, Nagano N, Kohmoto T. Coronary artery bypass grafting in the elderly. Chest. 2000;117(5):1262-70. [
MedLine]
2. Herlitz J, Brandrup-Wognsen G, Karlsson T, Karlson B, Haglid M, Sjoland H. Predictors of death and other cardiac events within 2 years after coronary artery bypass grafting. Cardiology. 1998;90(2):110-4. [
MedLine]
3. Mangano CM, Diamondstone LS, Ramsay JG, Aggarwal A, Herskowitz A, Mangano DT. Renal dysfunction after myocardial revascularization: risk factors, adverse outcomes, and hospital resource utilization. The Multicenter Study of Perioperative Ischemia Research Group. Ann Intern Med. 1998;128(3):194-203. [
MedLine]
4. Provenchere S, Plantefeve G, Hufnagel G, Vicaut E, De Vaumas C, Lecharny JB, et al. Renal dysfunction after cardiac surgery with normothermic cardiopulmonary bypass: incidence, risk factors, and effect on clinical outcome. Anesth Analg. 2003;96(5):1258-64.
5. Chertow GM, Levy EM, Hammermeister KE, Grover F, Daley J. Independent association between acute renal failure and mortality following cardiac surgery. Am J Med. 1998;104(4):343-8. [
MedLine]
6. Chertow GM, Lazarus JM, Christiansen CL, Cook EF, Hammermeister KE, Grover F, et al. Preoperative renal risk stratification. Circulation. 1997;95(4):878-84. [
MedLine]
7. Sear JW. Kidney dysfunction in the postoperative period. Br J Anaesth. 2005;95(1):20-32. [
MedLine]
8. Mangos GJ, Brown MA, Chan WY, Horton D, Trew P, Whitworth JA. Acute renal failure following cardiac surgery: incidence, outcomes and risk factors. Aust N Z J Med. 1995;25(4):284-9. [
MedLine]
9. Byers J, Sladen RN. Renal function and dysfunction. Curr Opin Anesthesiol. 2001;14(6):699-706.
10. Van der Wal RM, van Brussel BL, VoorsAA, Smilde TD, Kelder JC, van Swieten HA, et al. Mild preoperative renal dysfunction as a predictor of long-term clinical outcome after coronary bypass surgery. J Thorac Cardiovasc Surg. 2005,129(2):330-5. [
MedLine]
11. Zakeri R, Freemantle N, Barnett V, Lipkin GW, Bonser RS, Graham TR, et al. Relation between mild renal dysfunction and outcomes after coronary artery bypass grafting. Circulation. 2005;112(9 suppl.):I270-5. [
MedLine]
12. Boldt J, Brenner T, Lehmann A, Suttner SW, Kumle B, Isgro F. Is kidney function altered by the duration of cardiopulmonary bypass? Ann Thorac Surg. 2003;75(3):906-12. [
MedLine]
13. Ostermann ME, Taube D, Morgan CJ, Evans TW. Acute renal failure following cardiopulmonary bypass: a changing picture. Intensive Care Med. 2000;26(5):565-71. [
MedLine]
14. Conlon PJ, Sttaford-Smith M, White WD, Newman MF, King S,Winn MP, et al. Acute renal failure following cardiac surgery. Nephrol Dial Transplant. 1999;14(5):1158-62. [
MedLine]
15. Hammermeister KE, Burchfiel C, Johnson R, Grover FL. Identification of patients at greatest risk for developing major complications at cardiac surgery. Circulation. 1990;82( 5 suppl):IV380-9. [
MedLine]
16. Reston JT, Tregear SJ, Tukelson CM. Meta-analysis of short-term and mid-term outcomes following off-pump coronary artery bypass grafting. Ann Thorac Surg. 2003;76(5):1510-5. [
MedLine]
17. Morgera S, Woydt R, Kern H, Schmutzler M, DeJonge K, Lun A, et al. Low-dose prostacyclin preserves renal function in high-risk patients after coronany bypass surgery. Crit Care Med. 2002;30(1):107-12. [
MedLine]
18. Hall RI, Smith MS, Rocker G. The systemic inflammatory response to cardiopulmonary bypass: pathophysiological, therapeutic and pharmacological considerations. Anesth Analg. 1997;85(4):766-82. [
MedLine]
19. de Vroege R, van Oeveren W, van Klarenbosch J, Stooker W, Huybregts MA, Hack CE, et al. The impact of heparin-coated cardiopulmonary bypass circuits on pulmonary function and the release of inflammatory mediators. Anesth Analg. 2004;98(6):1586-94.
20. Whitten CW, Hill GE, Ivy R, Greilich PE, Lipton JM. Does the duration of cardiopulmonary bypass or aortic cross-clamp, in the absence of blood and/or blood product administration, influence the IL-6 response to cardiac surgery? Anesth Analg. 1998;86(1):28-33. [
MedLine]
21. Bronden B, Dencker M, Allers M, Plaza I, Jonsson H. Differential distribution of lipid microemboli after cardiac surgery. Ann Thorac Surg. 2006;81(2):643-8. [
MedLine]
22. Abu-Omar Y, Balacumaraswami L, Pigott DW, Matthews PM, Taggart DP. Solid and gaseous cerebral microembolization during off-pump, on-pump, and open cardiac surgery procedures. J Thorac Cardiovasc Surg. 2004;127(6):1759-65. [
MedLine]
23. Bucerius J, Gummert JF, Walther T, Schmitt DV, Doll N, Falk V, et al. On-pump versus off-pump coronary artery bypass grafting: impact on postoperative renal failure requiring renal replacement therapy. Ann Thorac Surg. 2004;77(4):1250-6. [
MedLine]
24. Ascione R, Lloyd CT, Underwood MJ, Gomes WJ, Angelini GD. On-pump versus off-pump coronary revascularization: evaluation of renal function. Ann Thorac Surg. 1999;68(2):493-8. [
MedLine]



 All scientific articles published at bjcvs.org are licensed under a Creative Commons license
All scientific articles published at bjcvs.org are licensed under a Creative Commons license